填空题 适中0.65 引用5 组卷91
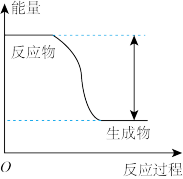
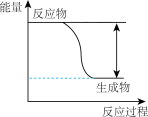
反应Fe+H2SO4 FeSO4+H2↑的能量变化趋势如图所示:
FeSO4+H2↑的能量变化趋势如图所示:
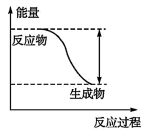
(1)该反应为____ (填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率增大,下列措施可行的是____ (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸
C.升高温度 D.减小压强
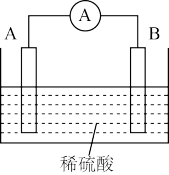
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为____ (填“正”或“负”)极。铜片上产生的现象为_________ ,该极上发生的电极反应为_______________ ,外电路中电子由____ (填“正”或“负”,下同)极向____ 极移动。

(1)该反应为
(2)若要使该反应的反应速率增大,下列措施可行的是
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸
C.升高温度 D.减小压强
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
18-19高一下·辽宁营口·阶段练习
类题推荐
反应Fe+H2SO4=FeSO4+H2↑的能量变化如图所示,请回答下列问题:
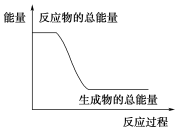
(1)该反应为_______ 反应选(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是_______(填字母)。
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜极上发生的电极反应为_______ ,另一个电极的材料是_______ (填名称),该电极上发生的电极反应为_______ ,外电路中电子由_______ 极(选填“正”或“负”,下同)向_______ 极移动,电解质溶液中的阴离子向_______ 极移动。

(1)该反应为
(2)若要使该反应的反应速率加快,下列措施可行的是_______(填字母)。
| A.改铁片为铁粉 |
| B.改稀硫酸为98%的浓硫酸 |
| C.升高温度 |
| D.将2.4 mol·L-1的稀硫酸改为4.8 mol·L-1稀盐酸 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网