单选题 适中0.65 引用2 组卷117
一定温度下,向 溶液中加入适量
溶液中加入适量 溶液,不同时刻测得生成
溶液,不同时刻测得生成 的体积(已折算为标准状况)如下表所示。资料显示,反应分两步进行:①
的体积(已折算为标准状况)如下表所示。资料显示,反应分两步进行:① ,②
,② ,反应过程中能量变化如下图所示。下列说法正确的是( )
,反应过程中能量变化如下图所示。下列说法正确的是( )


| t/min | 0 | 3 | 6 | 10 |
| V(O2)/mL | 0 | 9.9 | 17.2 | 22.4 |
| A. |
| B.0~10 min的平均反应速率: |
| C.反应 |
| D.反应 |
20-21高三上·四川南充·期中
类题推荐
向 20mL0.40mol·L-1H2O2 溶液中加入少量 KI 溶液,反应历程是:ⅰ.H2O2+I-=H2O+IO﹣;ⅱ.H2O2+IO﹣=H2O+O2↑+I﹣。H2O2分解反应过程中能量变化和不同时刻测得生成 O2 的体积(已折算为标准状况)如下图所示。
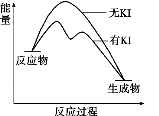
下列说法不正确的是
| t/min | 0 | 5 | 10 | 15 | 20 |
| V(O2)/mL | 0.0 | 12.6 | 20.16 | 28.0 | 32.7 |

下列说法不正确的是
| A.KI 是 H2O2 分解反应的催化剂 |
| B.KI 的加入改变了 H2O2 分解反应的反应历程 |
| C.KI 的加入降低了反应的活化能,因此提高了反应速率 |
| D.0~10min 的平均反应速率:v(H2O2)≈4.0×10-3mol/(L·min) |
某研究小组设计了如下实验,探究常温下催化剂对过氧化氢分解反应的影响。
(1)实验Ⅰ的作用是_______________ 。
(2)实验Ⅲ中反应的化学方程式为_______________ 。
(3)根据实验Ⅰ~Ⅲ中现象的不同,可以得出的结论是:
①使用合适的催化剂,可提高双氧水分解的反应速率;
②_______________ 。
(4)在一定温度下,10 mL 0.40 mol/L,H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表所示:
0~6 min,以H2O2的浓度变化表示的反应速率为v(H2O2)=_________ mol/(L·min)。(计算结果精确到0.001)
| Ⅰ | Ⅱ | Ⅲ | |
| 实验操作 示意图 | 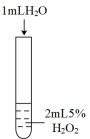 | 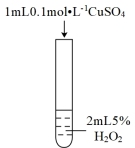 | 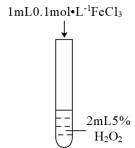 |
| 实验现象 | 有极少量气泡产生 | 产生气泡速率略有加快 | 产生气泡速率明显加快 |
(2)实验Ⅲ中反应的化学方程式为
(3)根据实验Ⅰ~Ⅲ中现象的不同,可以得出的结论是:
①使用合适的催化剂,可提高双氧水分解的反应速率;
②
(4)在一定温度下,10 mL 0.40 mol/L,H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表所示:
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
在一定温度下,10 mL 0.40 mol/L H2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表。忽略溶液体积变化,下列叙述不正确的是
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.6 | 16.8 | 22.4 | 26.5 | 29.9 |
| A.该反应可用MnO2、FeCl3溶液作为催化剂 |
| B.0~4 min的平均反应速率v(H2O2)=3.75×10-2mol/(L·min) |
| C.0~10 min,过氧化氢的分解速率逐渐加快 |
| D.反应到6 min时,H2O2分解了50% |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


