解答题-工业流程题 较难0.4 引用2 组卷472
钒和五氧化二钒在工业应用中广泛,某工厂从钒渣中回收金属,钒渣中主要成分有V2O3、FeO,还含有少量的CuO、Al2O3,工艺流程如图:
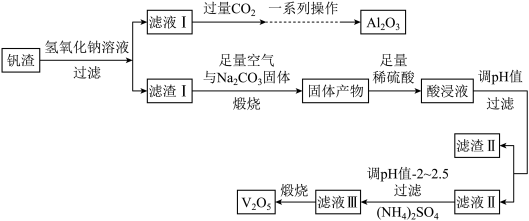
已知:①KspCu(OH)2=1.0×10−21;KspFe(OH)3=4.0×10−38;KspFe(OH)2=8.0×10−16。
②NH4VO3难溶于水,(VO2)2SO4易溶于水。
(1)写出滤液I中加入过量的CO2时发生反应的离子方程式;制取纯净的Al2O3需要经过一系列操作:过滤、___ 、___ 。
(2)煅烧时,滤渣I的主要成分V2O3转化为可溶性NaVO3,写出其反应的化学方程式___ 。
(3)加入稀硫酸后,酸浸液中VO3−与VO2+能大量共存的原因是___ (用离子方程式解释)。
(4)常温下调节酸浸液的pH=___ ,即可以完全除去铁、铜两种元素对应的离子___ ;实际pH值要调整到8,其目的是___ ;调pH=2~2.5后过滤,滤渣III的主要成分为___ 。
(5)请写出煅烧滤渣III时,发生反应的化学方程式___ 。

已知:①KspCu(OH)2=1.0×10−21;KspFe(OH)3=4.0×10−38;KspFe(OH)2=8.0×10−16。
②NH4VO3难溶于水,(VO2)2SO4易溶于水。
(1)写出滤液I中加入过量的CO2时发生反应的离子方程式;制取纯净的Al2O3需要经过一系列操作:过滤、
(2)煅烧时,滤渣I的主要成分V2O3转化为可溶性NaVO3,写出其反应的化学方程式
(3)加入稀硫酸后,酸浸液中VO3−与VO2+能大量共存的原因是
(4)常温下调节酸浸液的pH=
(5)请写出煅烧滤渣III时,发生反应的化学方程式
2020·江西·模拟预测
类题推荐
五氧化二钒(V2O5)在冶金、催化剂、磁性材料等领域有重要作用。实验室以含钒废料(含有V2O3、Fe2O3、Al2O3、CuO、有机物等)来制备V2O5的一种工艺流程如下:
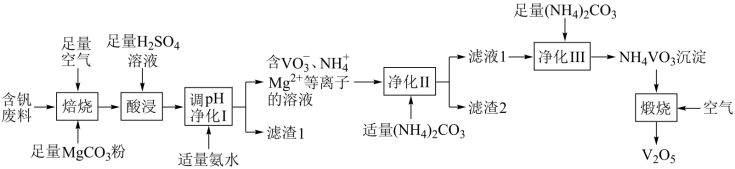
已知:含钒离子在溶液中的主要存在形式与溶液pH的关系:
请回答下列问题:
(1)含钒废料中的有机物主要在___________ 工序中除去。
(2)“焙烧”产物之一是Mg(VO3)2,写出它在“酸浸”(溶液pH<2)过程中发生反应的化学方程式___________ 。
(3)常温时,若“调pH净化I”工序中最终溶液pH=7,通过计算判断,此时Cu2+是否已经沉淀完全(已知离子浓度<1.0×10﹣5mol·L﹣1认为沉淀完全;Ksp[Cu(OH)2]=4.8×10﹣30)___________ 。
(4)“净化Ⅱ”时若加入过量的(NH4)2CO3,可能导致的后果为___________ 。
(5)“滤渣2”中含有Mg2(OH)2CO3,写出生成Mg2(OH)2CO3的离子方程式___________ 。
(6)“煅烧”时,除生成V2O5外,还生成了参与大气循环的气体,写出煅烧时的化学方程式___________ 。

已知:含钒离子在溶液中的主要存在形式与溶液pH的关系:
| 溶液pH | <4.0 | 6.0—8.0 | 8.0—10.0 |
| 钒元素主要存在形式 |
(1)含钒废料中的有机物主要在
(2)“焙烧”产物之一是Mg(VO3)2,写出它在“酸浸”(溶液pH<2)过程中发生反应的化学方程式
(3)常温时,若“调pH净化I”工序中最终溶液pH=7,通过计算判断,此时Cu2+是否已经沉淀完全(已知离子浓度<1.0×10﹣5mol·L﹣1认为沉淀完全;Ksp[Cu(OH)2]=4.8×10﹣30)
(4)“净化Ⅱ”时若加入过量的(NH4)2CO3,可能导致的后果为
(5)“滤渣2”中含有Mg2(OH)2CO3,写出生成Mg2(OH)2CO3的离子方程式
(6)“煅烧”时,除生成V2O5外,还生成了参与大气循环的气体,写出煅烧时的化学方程式
一种以转炉钒渣(主要成分为V2O3、FeO、SiO2及少量MgO、CaO、Al2O3)为原料实现低成本回收钒资源的生产工艺如下:
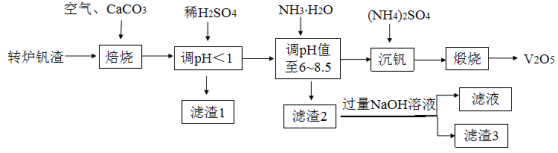
表一:相关金属离子[c0(Mn+)=0.01mol·L−1]形成氢氧化物沉淀的pH范围如下:
表二:部分含钒物质在水溶液中主要存在形式如下:
已知:①“焙烧”的主要反应为:CaCO3(s)=CaO(s)+CO2(g);
②在焙烧过程中产生Ca2V2O7;其中,Ca2V2O7在水中的溶解度小,易溶于稀硫酸和碱溶液。
回答下列问题:
(1)Ca2V2O7中V的化合价为_______ ,写出流程中氧化“钒”的化学方程式_______ 。
(2)“酸浸”后钒元素主要以VO 存在,生成VO
存在,生成VO 的离子方程式为
的离子方程式为_______ 。
(3)“滤渣2”的主要成分是_______ 。
(4)“调pH”中一般控制温度不超过40℃,原因是_______ 。
(5)利用上述表格数据,计算Fe(OH)3的Ksp=_______ 。
(6)已知“沉钒”得到NH4VO3,该环节通常需要加入过量(NH4)2SO4,其原因是_______ 。
(7)滤液经浓缩后,经电解后得到高纯度的氢氧化物,该反应阴极电极反应式为_______ 。

表一:相关金属离子[c0(Mn+)=0.01mol·L−1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀的pH | 7.5 | 2.2 | 3.7 | 9.4 |
| 沉淀完全的pH | 9.0 | 3.2 | 4.7 | 10.9 |
| pH | <1 | 1~4 | 6~8.5 | >13 |
| 主要形式 | VO | V2O5 | VO | VO |
| 备注 | 多钒酸盐在水中溶解度较小 | |||
②在焙烧过程中产生Ca2V2O7;其中,Ca2V2O7在水中的溶解度小,易溶于稀硫酸和碱溶液。
回答下列问题:
(1)Ca2V2O7中V的化合价为
(2)“酸浸”后钒元素主要以VO
(3)“滤渣2”的主要成分是
(4)“调pH”中一般控制温度不超过40℃,原因是
(5)利用上述表格数据,计算Fe(OH)3的Ksp=
(6)已知“沉钒”得到NH4VO3,该环节通常需要加入过量(NH4)2SO4,其原因是
(7)滤液经浓缩后,经电解后得到高纯度的氢氧化物,该反应阴极电极反应式为
五氧化二钒(V2O5)在冶金、催化剂、磁性材料等领域有重要作用。实验室以含钒废料(含有V2O3、Fe2O3、Al2O3、CuO、有机物等)来制备V2O5的一种工艺流程如下:
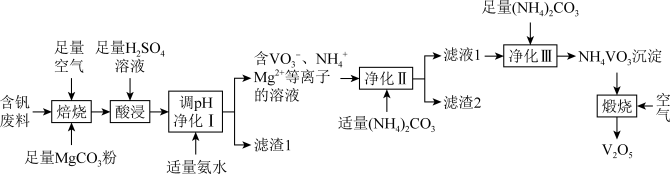
已知:含钒离子在溶液中的主要存在形式与溶液pH的关系:
请回答下列问题:
(1)pH<4.0时 中钒元素的化合价为
中钒元素的化合价为___________ 。
(2)含钒废料中的有机物主要在___________ 工序中除去。
(3)“焙烧”产物之一是 ,写出它在“酸浸”(溶液pH<2)过程中发生反应的化学方程式
,写出它在“酸浸”(溶液pH<2)过程中发生反应的化学方程式___________
(4)常温时,若“调pH净化I”工序中最终溶液pH=7,通过计算判断,此时Cu2+是否已经沉淀完全,并写出计算过程(已知离子浓度 认为沉淀完全;
认为沉淀完全;
___________ (填“是”或“否”),___________ 。
(5)“净化Ⅱ”时若加入过量的 ,可能导致的后果为
,可能导致的后果为___________ 。
(6)“滤渣2”中含有 ,写出生成
,写出生成 的离子方程式
的离子方程式___________ 。
(7)“煅烧”时,除生成V2O5外,还生成了参与大气循环的气体,写出煅烧时的化学方程式___________ 。

已知:含钒离子在溶液中的主要存在形式与溶液pH的关系:
| 溶液pH | <4.0 | 6.0—8.0 | 8.0—10.0 |
| 钒元素主要存在形式 |
请回答下列问题:
(1)pH<4.0时
(2)含钒废料中的有机物主要在
(3)“焙烧”产物之一是
(4)常温时,若“调pH净化I”工序中最终溶液pH=7,通过计算判断,此时Cu2+是否已经沉淀完全,并写出计算过程(已知离子浓度
(5)“净化Ⅱ”时若加入过量的
(6)“滤渣2”中含有
(7)“煅烧”时,除生成V2O5外,还生成了参与大气循环的气体,写出煅烧时的化学方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


