单选题 较易0.85 引用2 组卷119
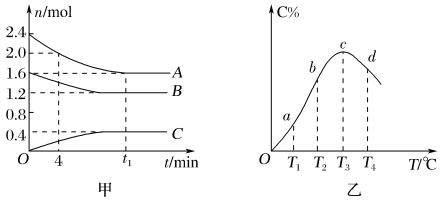
在10 L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图甲,C的百分含量与温度的关系如图乙。
下列分析不正确的是

下列分析不正确的是
| A.0~4 min时,A的平均反应速率为0.02 mol·L-1·min-1 |
| B.该反应的化学方程式为2A(g)+B(g)⇌C(g) |
| C.由T1向T2变化时,正反应速率大于逆反应速率 |
| D.该反应正反应是放热反应 |
19-20高二下·甘肃天水·开学考试
类题推荐
某温度时,在体积为1L的密闭容器中,A、B、C三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为Tl和T2时,B的体积百分含量与时间关系如图Ⅱ所示.则下列结论正确的是
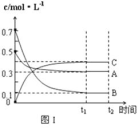
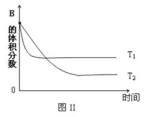


| A.该反应的热化学方程式为:A(g )+3B(g) ⇌2C(g);△H>0 |
| B.达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |
| C.达到平衡后,若其他条件不变,减小体积,平衡向逆反应方向移动 |
| D.若其它条件不变,升高温度,正、逆反应速率均增大,A的转化率减小 |
T ℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1℃和T2℃时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是:
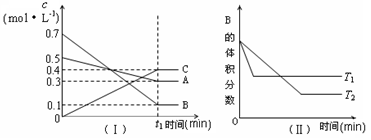
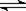

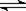
A.该平衡体系的化学反应方程式为:3A(g)+B(g) 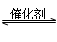 4C(g) 4C(g) |
| B.在t1时间内用B表示该反应的平均速率为0.6/t1 mol·L-1·min-1 |
| C.其他条件不变,升高温度,正反应速率减小、逆反应速率增大,A的转化率减小 |
| D.维持温度和容器体积不变,往平衡体系中充惰性气体,C的百分含量增大 |
T℃时,A、B 两种气体反应生成 C 气体。反应过程中 A、B、C 浓度变化如图(I)所示 , 若保持其他条件不变,温度分别为 T1和 T2时,B 的体积分数与时间的关系如图(II)所示 ,则下列结论正确的是 ( )


| A.该反应的热化学方程式 A(g)+2B(g)=2C(g)△H= -285.84kJ•mol-1 |
| B.该反应中 T1<T2 |
| C.其他条件不变,升高温度,正、逆反应速率均增大,且 A 的转化率增大 |
| D.T℃时,在相同容器中,若由 0.3 mol/L A、0.1 mol/L B 和 0.4 mol/L C 反 应,达到平衡后,C 的浓度仍为 0.4 mol/L |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


