单选题 适中0.65 引用25 组卷380
2SO2(g)+O2(g) ⇌2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是( )
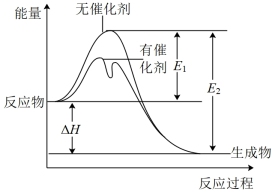

| A.该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数 |
| B.0℃、101kPa下,将1molSO2(g)和0.5molO2(g)置于密闭容器中充分反应生成SO3(g)放热akJ,其热化学方程式为2SO2(g)+O2(g) ⇌2SO3(g) ΔH=-2akJ·mol-l |
| C.该反应中,反应物的总键能小于生成物的总键能 |
| D.ΔH=E1-E2,使用催化剂改变活化能,但不改变反应热 |
2018·湖南·一模
知识点:根据△H=反应物的键能之和-生成物的键能之和进行计算根据△H=生成物的总能量之和-反应物的总能量之和进行计算碰撞理论及活化能催化剂对化学反应速率的影响 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录
类题推荐  反应过程中的能量变化如图所示(图中
反应过程中的能量变化如图所示(图中 表示无催化剂时正反应的活化能,
表示无催化剂时正反应的活化能, 表示无催化剂时逆反应的活化能)。下列有关叙述正确的是
表示无催化剂时逆反应的活化能)。下列有关叙述正确的是
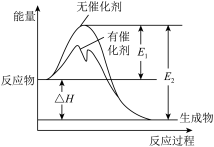
2SO2(g)+O2(g) 2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是
2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是

| A.该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数 |
| B.该反应的反应热ΔH=E1-E2 |
| C.该反应中,反应物的总能量小于生成物的总能量 |
| D.使用催化剂改变活化能,同时也改变反应热 |
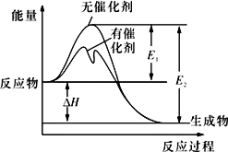
2SO2(g)+O2(g)  2SO3(g)反应过程中能量变化如图所示,下列有关叙述正确的是
2SO3(g)反应过程中能量变化如图所示,下列有关叙述正确的是


| A.该反应的逆反应为放热反应,升高温度可提高活化分子的百分数 |
| B.ΔH=E1-E2,使用催化剂可降低反应的反应热 |
| C.该反应中,反应物的总键能大于生成物的总键能 |
| D.若1molSO2与0.5molO2反应放热akJ,则相同条件2SO2(g)+O2(g) |

| A.该反应的逆反应为吸热反应, |
| B. |
| C.该反应中,反应物的总键能小于生成物的总键能 |
| D. |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


