解答题-实验探究题 适中0.65 引用4 组卷541
草酸铁铵[(NH4)3Fe(C2O4)3]是一种常用的金属着色剂,易溶于水,常温下其水溶液的pH介于4.0~5.0之间。某兴趣小组设计实验制备草酸铁铵并测其纯度。
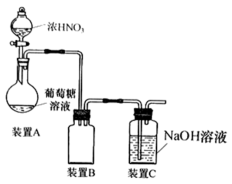
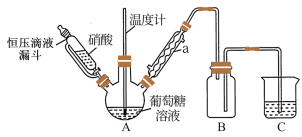
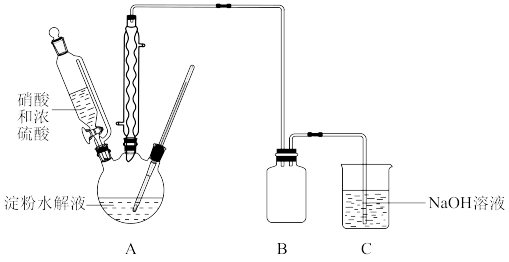
(1)甲组设计由硝酸氧化葡萄糖制取草酸,其实验装置(夹持及加热装置略去)如图所示。
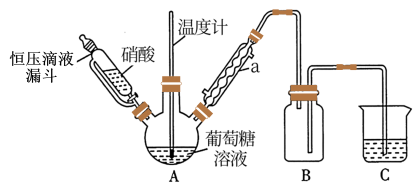
①仪器a的名称是________________ 。
②55~60℃下,装置A中生成H2C2O4,同时生成NO2和NO且物质的量之比为3:1,该反应的化学方程式为__________________________ 。
③装置B的作用是______________________ ;装置C中盛装的试剂是______________ 。
(2)乙组利用甲组提纯后的草酸溶液制备草酸铁铵。
将Fe2O3在搅拌条件下溶于热的草酸溶液;滴加氨水至__________ ,然后将溶液________ 、过滤、洗涤并干燥,制得草酸铁铵产品。
(3)丙组设计实验测定乙组产品的纯度。
准确称量5.000g产品配成100mL溶液,取10.00mL于锥形瓶中,加入足量0.1000mol·L-1稀硫酸酸化后,再用0.1000mol·L-1KMnO4标准溶液进行滴定,消耗KMnO4溶液的体积为12.00mL。
①滴定终点的现象是_______________________ 。
②滴定过程中发现褪色速率开始缓慢后迅速加快,其主要原因是____________________ 。
③产品中(NH4)3Fe(C2O4)3的质量分数为____________ %。[已知:(NH4)3Fe(C2O4)3的摩尔质量为374g·mol-1]
(1)甲组设计由硝酸氧化葡萄糖制取草酸,其实验装置(夹持及加热装置略去)如图所示。

①仪器a的名称是
②55~60℃下,装置A中生成H2C2O4,同时生成NO2和NO且物质的量之比为3:1,该反应的化学方程式为
③装置B的作用是
(2)乙组利用甲组提纯后的草酸溶液制备草酸铁铵。
将Fe2O3在搅拌条件下溶于热的草酸溶液;滴加氨水至
(3)丙组设计实验测定乙组产品的纯度。
准确称量5.000g产品配成100mL溶液,取10.00mL于锥形瓶中,加入足量0.1000mol·L-1稀硫酸酸化后,再用0.1000mol·L-1KMnO4标准溶液进行滴定,消耗KMnO4溶液的体积为12.00mL。
①滴定终点的现象是
②滴定过程中发现褪色速率开始缓慢后迅速加快,其主要原因是
③产品中(NH4)3Fe(C2O4)3的质量分数为
2020·山东临沂·一模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网