解答题-原理综合题 适中0.65 引用2 组卷246
锰及其化合物在现代工业、农业生产中有着广泛的应用,同时也是实验室中常用的重要试剂。
(1)KMnO4是强氧化剂,其溶液中c(H+)=c(OH-),则常温下0.01mol•L-1的HMnO4溶液的pH=_____________ 。
(2)MnS常用于除去污水中的Pb2+等重金属离子:Pb2+(aq)+ MnS(s)⇌PbS(s)+Mn2+(aq),若经过处理后的水中c(Mn2+)=1 ×10-6 mol•L-1,则c(Pb2+)=______________ [已知Ksp(PbS)=8×10-28、Ksp(MnS)=2×10-13]。
(3)锰是农作物生长的重要微量元素,用硫酸锰溶液拌种可使农作物产量提高10%~15%。某工厂利用回收的废旧锌锰干电池生成硫酸锰晶体(MnSO4•H2O)的流程如图所示:
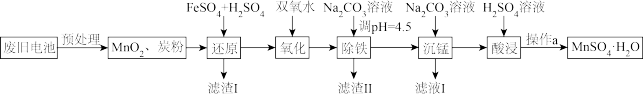
①MnSO4中含有的化学键类型有_______________ 。
②滤渣Ⅱ的主要成分是____________ ,滤渣Ⅰ是一种黑色单质,“还原”过程中氧化产物是Fe3+,写出相应反应的离子方程式_________ ,此反应中MnO2的转化率与温度之间的关系如图所示,则适宜的温度是______________ (填字母)。
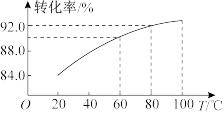
a.40 ℃ b.60 ℃ c.80 ℃ d.100 ℃
③“沉锰”中有无色无味的气体生成,还有MnCO3•6Mn(OH)2•5H2O生成,写出相应反应的化学方程式_________ 。
(1)KMnO4是强氧化剂,其溶液中c(H+)=c(OH-),则常温下0.01mol•L-1的HMnO4溶液的pH=
(2)MnS常用于除去污水中的Pb2+等重金属离子:Pb2+(aq)+ MnS(s)⇌PbS(s)+Mn2+(aq),若经过处理后的水中c(Mn2+)=1 ×10-6 mol•L-1,则c(Pb2+)=
(3)锰是农作物生长的重要微量元素,用硫酸锰溶液拌种可使农作物产量提高10%~15%。某工厂利用回收的废旧锌锰干电池生成硫酸锰晶体(MnSO4•H2O)的流程如图所示:

①MnSO4中含有的化学键类型有
②滤渣Ⅱ的主要成分是

a.40 ℃ b.60 ℃ c.80 ℃ d.100 ℃
③“沉锰”中有无色无味的气体生成,还有MnCO3•6Mn(OH)2•5H2O生成,写出相应反应的化学方程式
20-21高三上·四川眉山·阶段练习
类题推荐
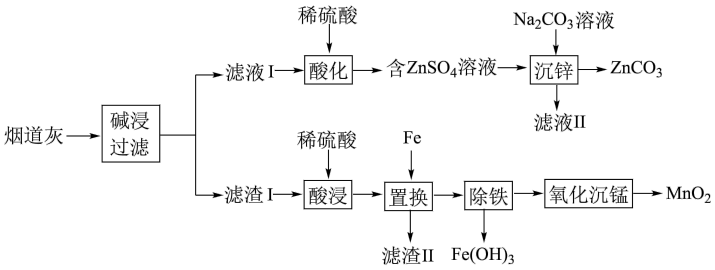
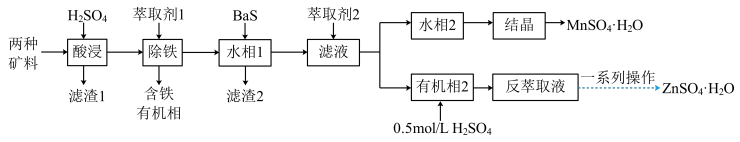
利用锌精矿(ZnS)和软锰矿(MnO2)两种矿料(含少量杂质Fe、 Cu、 Pb等元素的化合物及SiO2)生产硫酸锌和硫酸锰的流程如下:
②Ksp(ZnS)=2.0 ×10-22, Ksp(MnS)=2.0 ×10-13;
③ZnSO4的溶解度如表所示
回答下列问题:
(1)“滤渣1”主要成分为_______ 、S;写出“酸浸”过程的主要离子方程式_______ 。
(2)“除铁”的萃取剂为磷酸二(2-乙基己基)酯(用HA表示),萃取后含铁的物质为[Fe(HA)2(H2O)2]ASO4,该物质中Fe3+的配位数为_______ 。
(3)BaS 为可溶性钡盐。向“水相1”中加入适量BaS目的是_______ ;溶液 pH过高,会造成Zn2+、Mn2+沉淀而损失,若溶液中Zn2+、Mn2+的浓度为0.2mol·L-1,则应控制溶液中c(H+)大于_______ mol·L-1。
(4)从“反萃取液”中获得ZnSO4·H2O晶体的操作为:控制温度在_______ °C以 上蒸发结晶、_______ 、洗涤、干燥。
(5)含50% MnO2的软锰矿174t,利用此工艺获得MnSO4·H2O160.55t,该工艺MnSO4·H2O的产率为_______ 。
②Ksp(ZnS)=2.0 ×10-22, Ksp(MnS)=2.0 ×10-13;
③ZnSO4的溶解度如表所示
| 水/温度(°C) | 0 | 10 | 20 | 25 | 40 | 50 | 60 | 70 | 80 | 90 |
| ZnSO4 | 41.8 | 47.5 | 54.1 | 58.0 | 62.1 | 74.8 | 67.2 | 60.5 | 一 | 一 |
| ZnSO4·H2O | 41.9 | 一 | 54.2 | 一 | 一 | 74.0 | 一 | 一 | 86.6 | 83.5 |
| ZnSO4·6H2O | 一 | 一 | 一 | 一 | 70.1 | 76.8 | 一 | 一 | 一 | 一 |
| ZnSO4·7H2O | 41.9 | 47.0 | 54.4 | 58.0 | 一 | 一 | 一 | 一 | 一 | 一 |
(1)“滤渣1”主要成分为
(2)“除铁”的萃取剂为磷酸二(2-乙基己基)酯(用HA表示),萃取后含铁的物质为[Fe(HA)2(H2O)2]ASO4,该物质中Fe3+的配位数为
(3)BaS 为可溶性钡盐。向“水相1”中加入适量BaS目的是
(4)从“反萃取液”中获得ZnSO4·H2O晶体的操作为:控制温度在
(5)含50% MnO2的软锰矿174t,利用此工艺获得MnSO4·H2O160.55t,该工艺MnSO4·H2O的产率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网