单选题 较易0.85 引用2 组卷130
反应2C+O2=2CO的能量变化如图所示。下列说法正确的是( )
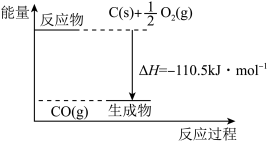

| A.12gC(s)与一定量O2(g)反应生成14gCO(g)放出的热量为110.5kJ |
| B.2molC(s)与足量O2(g)反应生成CO2(g)放出的热量大于221kJ |
| C.该反应的热化学方程式是2C(s)+O2(g)=2CO(g) ΔH=-221kJ |
| D.该反应的反应热等于生成的CO(g)中所具有的能量与参加反应的O2(g)中所具有的能量的差 |
19-20高一·全国·单元测试
类题推荐
反应2C(s)+O2(g)=2CO(g)的能量变化如图所示,下列说法正确的是
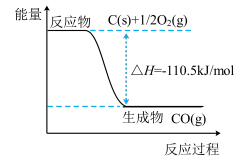

| A.生成物的总能量大于反应物的总能量 |
| B.∆H<0,表明该反应在常温下一定能发生 |
| C.2molC(s)与足量O2(g)反应生成CO2(g),放出的热量大于221kJ |
| D.该反应的热化学方程式是:2C(s)+O2(g)=2CO(g)ΔH=-110.5kJ/mol |
反应2C + O2=2CO 的能量变化如右图所示。含11.2g KOH的稀溶液与1L0.1mol/L的H2SO4溶液反应放出11.46kJ的热量,下列说法正确的是
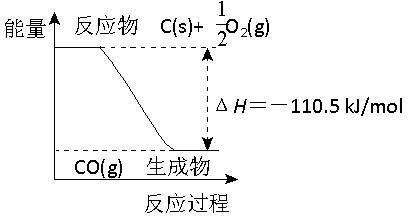

| A.2 mol C(s)与足量O2(g)反应生成CO2(g),放出的热量大于221 kJ 1 |
| B.12 g C(s)与一定量O2(g)反应生成14 g CO(g),放出的热量为110.5 kJ |
| C.该反应的热化学方程式是:2C(s) + O2(g)=2CO(g) ΔH=-110.5 kJ/mol |
| D.表示中和热的热化学方程式2KOH(aq)+H2SO4(aq)=K2SO4(aq)+2H2O(l)ΔH=-114.6 kJ/mol |
根据如下能量关系示意图,判断下列说法正确的是
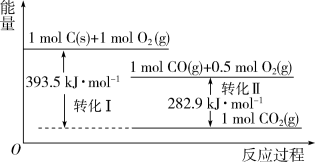

| A.1molC(s)与1molO2(g)的能量之和为393.5kJ |
| B.反应2CO(g)+O2(g)=2CO2(g)中,生成物的总能量大于反应物的总能量 |
| C.由C(s)→CO(g)的热化学方程式为2C(s)+O2(g)=2CO(g) ΔH=-110.6kJ·mol-1 |
| D.热值指一定条件下单位质量的物质完全燃烧所放出的热量,则CO的热值为10.1kJ·g-1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


